+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
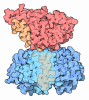
| タイトル | Composite cryo-EM map of the Chlamydomonas reinhardtii mastigoneme | |||||||||||||||||||||
 マップデータ マップデータ | Composite cryo-EM map of the C. reinhardtii mastigoneme | |||||||||||||||||||||
 試料 試料 |
| |||||||||||||||||||||
 キーワード キーワード |  Mastigoneme / Mastigoneme /  cilia (繊毛) / cilia (繊毛) /  STRUCTURAL PROTEIN (タンパク質) STRUCTURAL PROTEIN (タンパク質) | |||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | |||||||||||||||||||||
| 生物種 |   Chlamydomonas reinhardtii (クラミドモナス) Chlamydomonas reinhardtii (クラミドモナス) | |||||||||||||||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.1 Å クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||||||||||||||
 データ登録者 データ登録者 | Dai J / Ma M / Zhang R / Brown A | |||||||||||||||||||||
| 資金援助 |  米国, 6件 米国, 6件
| |||||||||||||||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2024 ジャーナル: Cell / 年: 2024タイトル: Mastigoneme structure reveals insights into the O-linked glycosylation code of native hydroxyproline-rich helices. 著者: Jin Dai / Meisheng Ma / Qingwei Niu / Robyn J Eisert / Xiangli Wang / Poulomi Das / Karl F Lechtreck / Susan K Dutcher / Rui Zhang / Alan Brown /  要旨: Hydroxyproline-rich glycoproteins (HRGPs) are a ubiquitous class of protein in the extracellular matrices and cell walls of plants and algae, yet little is known of their native structures or ...Hydroxyproline-rich glycoproteins (HRGPs) are a ubiquitous class of protein in the extracellular matrices and cell walls of plants and algae, yet little is known of their native structures or interactions. Here, we used electron cryomicroscopy (cryo-EM) to determine the structure of the hydroxyproline-rich mastigoneme, an extracellular filament isolated from the cilia of the alga Chlamydomonas reinhardtii. The structure demonstrates that mastigonemes are formed from two HRGPs (a filament of MST1 wrapped around a single copy of MST3) that both have hyperglycosylated poly(hydroxyproline) helices. Within the helices, O-linked glycosylation of the hydroxyproline residues and O-galactosylation of interspersed serine residues create a carbohydrate casing. Analysis of the associated glycans reveals how the pattern of hydroxyproline repetition determines the type and extent of glycosylation. MST3 possesses a PKD2-like transmembrane domain that forms a heteromeric polycystin-like cation channel with PKD2 and SIP, explaining how mastigonemes are tethered to ciliary membranes. | |||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_43892.map.gz emd_43892.map.gz | 27.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-43892-v30.xml emd-43892-v30.xml emd-43892.xml emd-43892.xml | 13.7 KB 13.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_43892.png emd_43892.png | 52.9 KB | ||
| Filedesc metadata |  emd-43892.cif.gz emd-43892.cif.gz | 4.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-43892 http://ftp.pdbj.org/pub/emdb/structures/EMD-43892 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43892 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43892 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_43892.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_43892.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Composite cryo-EM map of the C. reinhardtii mastigoneme | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.39 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Native mastigonemes
| 全体 | 名称: Native mastigonemes |
|---|---|
| 要素 |
|
-超分子 #1: Native mastigonemes
| 超分子 | 名称: Native mastigonemes / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Chlamydomonas reinhardtii (クラミドモナス) Chlamydomonas reinhardtii (クラミドモナス) |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 0.01 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 詳細: HMDEKP buffer (30 mM HEPES, 5 mM MgSO4, 1 mM DTT, 0.5 mM EGTA, 25 mM KCl, pH 7.4) containing 1x ProteaseArrest protease inhibitors (G-Biosciences) |
| グリッド | モデル: C-flat-1.2/1.3 / 材質: COPPER / メッシュ: 400 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 15 sec. / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 0.01 mm / 最大 デフォーカス(公称値): 3.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 81000 Bright-field microscopy / Cs: 0.01 mm / 最大 デフォーカス(公称値): 3.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 81000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 3838 pixel / デジタル化 - サイズ - 縦: 3710 pixel / 実像数: 19601 / 平均露光時間: 9.0 sec. / 平均電子線量: 38.9 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: OTHER / 詳細: ab initio by cryoSPARC |
|---|---|
| 初期 角度割当 | タイプ: PROJECTION MATCHING / ソフトウェア - 名称: cryoSPARC |
| 最終 3次元分類 | クラス数: 2 / ソフトウェア - 名称: cryoSPARC |
| 最終 角度割当 | タイプ: PROJECTION MATCHING / ソフトウェア - 名称: cryoSPARC (ver. 3.4) |
| 最終 再構成 | 使用したクラス数: 1 / 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: FOURIER SPACE / 解像度のタイプ: BY AUTHOR / 解像度: 3.1 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: cryoSPARC / 使用した粒子像数: 687452 |
-原子モデル構築 1
| 精密化 | プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-9b4h: |
 ムービー
ムービー コントローラー
コントローラー