+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8i47 | ||||||
|---|---|---|---|---|---|---|---|
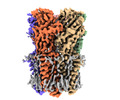
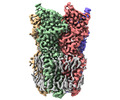
| タイトル | Cryo-EM structure of nanodisc (PE:PS:PC) reconstituted GLIC at pH 5.5 | ||||||
 要素 要素 | Proton-gated ion channel | ||||||
 キーワード キーワード |  MEMBRANE PROTEIN (膜タンパク質) / pentameric ligand-gated ion channels / cis-loop / MEMBRANE PROTEIN (膜タンパク質) / pentameric ligand-gated ion channels / cis-loop /  cryo-EM (低温電子顕微鏡法) / cryo-EM (低温電子顕微鏡法) /  nanodisc nanodisc | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 sodium channel activity / extracellular ligand-gated monoatomic ion channel activity / transmembrane transporter complex / sodium channel activity / extracellular ligand-gated monoatomic ion channel activity / transmembrane transporter complex /  potassium channel activity / potassium channel activity /  regulation of membrane potential / transmembrane signaling receptor activity / neuron projection / regulation of membrane potential / transmembrane signaling receptor activity / neuron projection /  シグナル伝達 / identical protein binding / シグナル伝達 / identical protein binding /  細胞膜 細胞膜類似検索 - 分子機能 | ||||||
| 生物種 |   Gloeobacter violaceus (バクテリア) Gloeobacter violaceus (バクテリア) | ||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.7 Å クライオ電子顕微鏡法 / 解像度: 2.7 Å | ||||||
 データ登録者 データ登録者 | Bharambe, N. / Li, Z. / Basak, S. | ||||||
| 資金援助 |  シンガポール, 1件 シンガポール, 1件
| ||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Cryo-EM structures of prokaryotic ligand-gated ion channel GLIC provide insights into gating in a lipid environment. 著者: Nikhil Bharambe / Zhuowen Li / David Seiferth / Asha Manikkoth Balakrishna / Philip C Biggin / Sandip Basak /   要旨: GLIC, a proton-activated prokaryotic ligand-gated ion channel, served as a model system for understanding the eukaryotic counterparts due to their structural and functional similarities. Despite ...GLIC, a proton-activated prokaryotic ligand-gated ion channel, served as a model system for understanding the eukaryotic counterparts due to their structural and functional similarities. Despite extensive studies conducted on GLIC, the molecular mechanism of channel gating in the lipid environment requires further investigation. Here, we present the cryo-EM structures of nanodisc-reconstituted GLIC at neutral and acidic pH in the resolution range of 2.6 - 3.4 Å. In our apo state at pH 7.5, the extracellular domain (ECD) displays conformational variations compared to the existing apo structures. At pH 4.0, three distinct conformational states (C1, C2 and O states) are identified. The protonated structures exhibit a compacted and counter-clockwise rotated ECD compared with our apo state. A gradual widening of the pore in the TMD is observed upon reducing the pH, with the widest pore in O state, accompanied by several layers of water pentagons. The pore radius and molecular dynamics (MD) simulations suggest that the O state represents an open conductive state. We also observe state-dependent interactions between several lipids and proteins that may be involved in the regulation of channel gating. Our results provide comprehensive insights into the importance of lipids impact on gating. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8i47.cif.gz 8i47.cif.gz | 341.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8i47.ent.gz pdb8i47.ent.gz | 281.4 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8i47.json.gz 8i47.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/i4/8i47 https://data.pdbj.org/pub/pdb/validation_reports/i4/8i47 ftp://data.pdbj.org/pub/pdb/validation_reports/i4/8i47 ftp://data.pdbj.org/pub/pdb/validation_reports/i4/8i47 | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  35163MC  8i41C  8i42C  8i48C  8jj3C  8wcqC  8wcrC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 35699.094 Da / 分子数: 5 / 由来タイプ: 組換発現 由来: (組換発現)   Gloeobacter violaceus (バクテリア) Gloeobacter violaceus (バクテリア)遺伝子: glvI / 発現宿主:   Escherichia coli (大腸菌) / 参照: UniProt: Q7NDN8 Escherichia coli (大腸菌) / 参照: UniProt: Q7NDN8#2: 化合物 | ChemComp-PEE /  Discrete optimized protein energy Discrete optimized protein energy#3: 水 | ChemComp-HOH / |  水 水研究の焦点であるリガンドがあるか | Y | |
|---|
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: pentameric ligand-gated ion channel / タイプ: COMPLEX / Entity ID: #1 / 由来: RECOMBINANT | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 由来(天然) | 生物種:   Gloeobacter violaceus (バクテリア) Gloeobacter violaceus (バクテリア) | ||||||||||||||||||||
| 由来(組換発現) | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) | ||||||||||||||||||||
| 緩衝液 | pH: 5.5 | ||||||||||||||||||||
| 緩衝液成分 |
| ||||||||||||||||||||
| 試料 | 濃度: 0.2 mg/ml / 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES | ||||||||||||||||||||
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil R1.2/1.3 | ||||||||||||||||||||
急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 1600 nm / 最小 デフォーカス(公称値): 800 nm / Cs Bright-field microscopy / 最大 デフォーカス(公称値): 1600 nm / 最小 デフォーカス(公称値): 800 nm / Cs : 2.7 mm : 2.7 mm |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 平均露光時間: 7 sec. / 電子線照射量: 57 e/Å2 / 検出モード: SUPER-RESOLUTION フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 実像数: 6625 |
| 電子光学装置 | エネルギーフィルタースリット幅: 20 eV |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 365137 | ||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性 : C5 (5回回転対称 : C5 (5回回転対称 ) ) | ||||||||||||||||||||||||||||||||||||||||
3次元再構成 | 解像度: 2.7 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 61526 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー





 PDBj
PDBj