+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Photorhabdus luminescens Makes caterpillars floppy (Mcf) toxin with the C-terminal deletion | |||||||||
 マップデータ マップデータ | The primary map that was used for model building | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  Bacterial toxin / Bacterial toxin /  TOXIN (毒素) TOXIN (毒素) | |||||||||
| 機能・相同性 | TcdA/TcdB toxin, pore forming domain / TcdA/TcdB pore forming domain /  Toxin protein Toxin protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Photorhabdus luminescens (バクテリア) Photorhabdus luminescens (バクテリア) | |||||||||
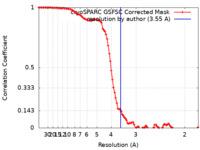
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.55 Å クライオ電子顕微鏡法 / 解像度: 3.55 Å | |||||||||
 データ登録者 データ登録者 | Belyy A / Heilen P / Hofnagel O / Raunser S | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: Structure and activation mechanism of the Makes caterpillars floppy 1 toxin. 著者: Alexander Belyy / Philipp Heilen / Philine Hagel / Oliver Hofnagel / Stefan Raunser /  要旨: The bacterial Makes caterpillars floppy 1 (Mcf1) toxin promotes apoptosis in insects, leading to loss of body turgor and death. The molecular mechanism underlying Mcf1 intoxication is poorly ...The bacterial Makes caterpillars floppy 1 (Mcf1) toxin promotes apoptosis in insects, leading to loss of body turgor and death. The molecular mechanism underlying Mcf1 intoxication is poorly understood. Here, we present the cryo-EM structure of Mcf1 from Photorhabdus luminescens, revealing a seahorse-like shape with a head and tail. While the three head domains contain two effectors, as well as an activator-binding domain (ABD) and an autoprotease, the tail consists of two putative translocation and three putative receptor-binding domains. Rearrangement of the tail moves the C-terminus away from the ABD and allows binding of the host cell ADP-ribosylation factor 3, inducing conformational changes that position the cleavage site closer to the protease. This distinct activation mechanism that is based on a hook-loop interaction results in three autocleavage reactions and the release of two toxic effectors. Unexpectedly, the BH3-like domain containing ABD is not an active effector. Our findings allow us to understand key steps of Mcf1 intoxication at the molecular level. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_17436.map.gz emd_17436.map.gz | 51.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-17436-v30.xml emd-17436-v30.xml emd-17436.xml emd-17436.xml | 19.5 KB 19.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_17436_fsc.xml emd_17436_fsc.xml | 9.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_17436.png emd_17436.png | 98 KB | ||
| マスクデータ |  emd_17436_msk_1.map emd_17436_msk_1.map | 103 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-17436.cif.gz emd-17436.cif.gz | 7.3 KB | ||
| その他 |  emd_17436_additional_1.map.gz emd_17436_additional_1.map.gz emd_17436_half_map_1.map.gz emd_17436_half_map_1.map.gz emd_17436_half_map_2.map.gz emd_17436_half_map_2.map.gz | 51.7 MB 95.6 MB 95.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-17436 http://ftp.pdbj.org/pub/emdb/structures/EMD-17436 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17436 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17436 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8p51MC  8p50C  8p52C M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_17436.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_17436.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | The primary map that was used for model building | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.9 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_17436_msk_1.map emd_17436_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
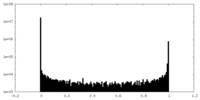
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: Local refinement map that was used to build...
| ファイル | emd_17436_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Local refinement map that was used to build the N-terminal effector region | ||||||||||||
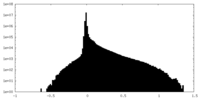
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: First half map
| ファイル | emd_17436_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | First half map | ||||||||||||
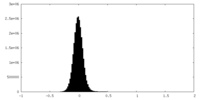
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Second half map
| ファイル | emd_17436_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Second half map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Photorhabdus luminescens Makes caterpillars floppy (Mcf) toxin wi...
| 全体 | 名称: Photorhabdus luminescens Makes caterpillars floppy (Mcf) toxin with the C-terminal deletion |
|---|---|
| 要素 |
|
-超分子 #1: Photorhabdus luminescens Makes caterpillars floppy (Mcf) toxin wi...
| 超分子 | 名称: Photorhabdus luminescens Makes caterpillars floppy (Mcf) toxin with the C-terminal deletion タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:   Photorhabdus luminescens (バクテリア) Photorhabdus luminescens (バクテリア) |
-分子 #1: Toxin protein
| 分子 | 名称: Toxin protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Photorhabdus luminescens (バクテリア) Photorhabdus luminescens (バクテリア) |
| 分子量 | 理論値: 325.211562 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 配列 | 文字列: MGSSHHHHHH SSGLVPRGSH MASISKDFTN LLNTLIDGQI GAASRQTEWF NMSPDERTDY IKQVDERLQE MQQSTLSVLA AQHFQMQDN PVSVGDQLQT LQKRRQQMTD VPGTPAINAY KQQLDRDILL YRRQQTAMTH FDSTWRKVLV MLGPDDSKPL N ATTLRENA ...文字列: MGSSHHHHHH SSGLVPRGSH MASISKDFTN LLNTLIDGQI GAASRQTEWF NMSPDERTDY IKQVDERLQE MQQSTLSVLA AQHFQMQDN PVSVGDQLQT LQKRRQQMTD VPGTPAINAY KQQLDRDILL YRRQQTAMTH FDSTWRKVLV MLGPDDSKPL N ATTLRENA VDKQAKLDTE IKRLEQQLTI QVADSTFSQK YVTLFSELQA YKDVNARYNA LLKASATEEA AALGALTKVP QA SDDLPVN ISLLMMEERP GYIRMNVALV NASTDGRFKD FFLENGRLVV LTDGVLNFSF GTAARSLAWQ QQYRLKSEPP SFR SPTYTP IRSVLVKTEF VEKYFANYLV SESTLRGGFK AQLLGNGRKM LLTSVDRKVP NQIGIQVSGQ APNTTITREV PLAS ALSDL INQNADIASF RTIGLEGFRQ SSYHPDRDGL FVNIHELERS VGFAGRQYLL EMPQDNDYLS ATPFGVMSVD GDKVS SSHL SKAQTDTLYQ YNAAFFEKLE QLRSGGMKAS RLFEGSIERT AFVQQLVRLL ERNHITPAGV LAPEYPRDNM RDIKGN NLN KVLWEQAFAA SVWRSRDNDP LLFRLATRLV KNPAVVKVLQ NGYVQSDIAQ ARELLAPLYE QWRTRAVEAE TQRVASA NA AQHPSNPKVH VFDQAEVERS LDDKLLILLL TGPQSLEGTD VQLRPMVEAA LLSNEGRSLR KQILFHALRP VADSFSKA A APVNPHAELG VGKIMINNRL NQPDPYLILN TSSEEQAYRD GSYLIKDDKY RSYNQFRPDF KNDATRYMND LDTPFVGGI SGTTQTVSNV LTELFGGALS VKQYWQFQMA NAAFMIRNGY HSFFETFYVA ARYEPEGADS IGKEMLQMFD KYRVEGSKKA LQGKLYDGV MARVLPIINQ GLSAADEFHP PRFTRIGPRP ALLGQAVKDL ELKAGLTSVG DGFEPRQGSA DIHQFVTDPV L FAKTHTVS AEALVRSGRL PAEGSAQLVK VGSGLYELEY TEQSANDISS SSIPAYFLGY NGPNQANAVP AYVDIPKRTI AG NFLFTGT LSGGSLVVTS LDANTFRVYH DGRVNSSLLY DNVVMAVDYK DYQIAGTAEG LAAAYMQYVN HEWQLVLQRQ EYQ RDGQML RLRLRDDEEP LSIQVADSQV VERNQAQFVA YREQIHQQLK KVATQFEVSI SGVSDGVYTE GEFSPDHPAI AAWA KLCAE VYDRINADTK QLVDKRNKLY ENRRNTIRRD LINQQIKQLN ITLEYYKAQY DTVLREAGFV EQSWLWQQIK AKNGS AAVV RIDDTAIQGG GKQRTDSVGE RYAISEAYQR GARGTGFSDG LRNFREIEIP GVDDKMSALE MKRLFLEGKL TSEQQG ALS GRITETSRAE YIDKVLRQTA VFSEDFHDAG SVFDRLVPQD FYLSLVGDRS GGRAYPLVRA MTVALASGGE AGINSLV QK LFFASADPQA GSSTLLRNSL IKLHSNVEAV QASTELGQFG LSEVVSRLAA TTGTSMFALN TQNHSMMVGS TVTTEGRR Y YFYDPNVGIF AFDNTKSLSR AMEQHLVGRR LAVHYGSFGS KSAPAFNLIE IDTGKMAEVP VGNGLNVADL TRFEELSSV IGQRRQVEQV MSAQERITED LQLSTALQAF DAEQWGARFE AASTRLAQEH QLDSRWLPII ATTEEQGEGR YRVQFINRDQ PEQTRWLDT DDSTFVEFRR FVDEHMSVLN EHFTLESGRM RPRGGVGEAA PVDGLNAGFA VQALIQWFSD KNRHDAANGM A SPDLATAL KVHSYLNFVQ MVHGGVQDVI KVTALVRTAL RGEVVAAQTS FKEFALSLGH TVNEGVGVLF GGAMIGLDAY EL AHAENDV QKAVFGTQLA FDSASFVTGA AGIGAGLVGA STAGAVLGGA GVILGGLAVG FTALAQAFGA VAEDAKAVGR YFD TVDKAY KGNGYRYDNE KQVLVPLAGA VIKTLDLSKN QIDFDSQYIY RTHSGSTGSG KINYFFWVGD FPRMVHDRGQ AIEV RSGIG YKDVSRPLEH GDSNVVILPG TPKSYISYEY MLLPGATTRH DAGFDVIRRL EEDKRFDYDF YIFPGEETIR RIHHE YVDT PIEVVLDQRN RQLVAPELPK ELHGFLCYEI KGAGGEYLIG LNEGAKVNLT SDVASTWIID SSQLASDSIS VSKDQL LVG EKGKEVVVKL YLAQNSQVLV VNGKGEVRKV DFTSLTAQVI SEDASKWQVP GQQIEQHLSD LAKAHQLHGQ YVVVENY RH QGRDVGRAFY DVTKDRMLFT DTTNEQAKRA QLGAVMGDYA YFYDADNAVA WRVDIATGQV DAQFEPWFNQ NAGHISRF W QEGDVVYLAR RYRLKEREAE LGYRIIGDRM ELVSAVGDDA LLQLSARIGR HGDELEAILQ GYRSNSTQRG TLMYTLGAR LIQPTSAALV TVFGVDAAGV PHRYWIRTSD GTLIKPNLAP PADQTLHFEA HEQTRSAWQI PADLVLAGSM PLLGGKEVFF FYSKEQKTL FRQEGPGQEV LDANQPSALR VTTPALTNVI NLNGHLVVVT EDGRVARLDA LGQLSYAAVN EHWLKGRIHW W QDLTSVTD GRATLAVFGV KDTDGKSLLP VWYHNGQVVV ASAALQDKHP QFLGFEVDGS SARLFEPASG KLYRQPAMTA DA LAAAFGT DEVLEASAQL PAANELEPEL HLKAAEQVDA GLRLTTVKGE ILLRTHDGKL QLVAVDKDWQ QDNLVRLSQA LAE VAGQWR VKGVLTLQGD DTQGWFDVGS GQVFSIGGIP ATDNLRFIGI AVGKKGAYVY NPTDQMLYQV KESGAQKLNH YADV ERIGS SLLLQDGGKG DLSPMLIAGV DSVVLHGGAG SDTYRLSQTM WSYYRTVVID NDDPNQVLDR LIILAVDAEK IFVSR HEDD LMLTDSVNGT VLVIRKVFGS QAVTHRHLQI DLEGSSSVIS VDHLVKGFTR UniProtKB:  Toxin protein Toxin protein |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| グリッド | モデル: C-flat-2/1 / 材質: COPPER / メッシュ: 400 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK III |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm Bright-field microscopy / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 撮影したグリッド数: 1 / 実像数: 9032 / 平均電子線量: 60.85 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-8p51: |
 ムービー
ムービー コントローラー
コントローラー










 Z
Z Y
Y X
X